Projektanslag 2018
The Birth of the Mitochondrial Ribosome
Huvudsökande:
Alexey Amunts, docent
Medsökande:
Karolinska Institutet
Martin Hallberg
Joanna Rorbach
Lärosäte:
Stockholms universitet
Beviljat anslag:
31,5 miljoner kronor under fem år
Alexey Amunts forskargrupp har ett femårigt projektanslag från Knut och Alice Wallenbergs Stiftelse för att visa oss delar av cellens universum i nanoskala.
– Med hjälp av den nya tekniken kryoelektronmikroskopi kan vi kartlägga hur mitoribosomerna skapas och även visualisera själva processen, säger Alexey Amunts.
Mitokondrier är våra cellers kraftverk som omvandlar föda till biokemisk energi som cellerna kan använda. Proteinerna som står för själva jobbet tillverkas på plats i mitokondrien, i särskilda proteinfabriker: mitoribosomerna. Dessa skiljer sig från kroppens övriga ribosomer genom att de enbart transkriberar den DNA-kod som finns i själva mitokondrien.
Alexey Amunts forskargrupp har gett sig i kast med uppgiften att förstå mitoribosomernas funktion och hur de egentligen skapas.
Explosiv utveckling
Vägen till förståelse börjar i ett källarrum på Albanova universitetscentrum i Stockholm. Här arbetar medlemmarna i Alexey Amunts forskargrupp med ett av landets två kryoelektronmikroskop. Utvecklingen av kryoelektronmikroskopi belönades med ett Nobelpris i kemi 2017. Tekniken gör det möjligt att avbilda molekyler som tredimensionella strukturer som sedan kan översättas till atommodeller. Denna teknik har gett livsvetenskaperna en närmast explosiv utveckling de senaste åren.
– Det är en mycket spännande tid att vara verksam inom vårt fält. Nästan varje dag klarlägger vi fundamentala förlopp i naturen enbart genom att titta på dem med hjälp av den nya kryotekniken, säger Alexey Amunts.
Själv lämnade han labbet i Cambridge, som var en av de platser där kryomikroskopin utvecklades, för att bygga upp forskningen i Sverige.
Han jämför utvecklingen av kryoelektronmikroskopi med utvecklingen av mikroskopet under slutet av 1600-talet. Det var först när holländaren Antonie van Leeuwenhoek uppfunnit det första mikroskopet som insikten kom att en organism bestod av celler.
– Mikroskopet gjorde att vi kunde se byggnadsblocken som bildar levande organismer. Nu kan vi titta på insidan av dem – i nanoskala. Och vad vi ser berättar hur molekylerna är utformade, hur de fungerar och arbetar tillsammans för att mitokondrien ska kunna omvandla den energi som upprätthåller liv.
Båda av landets två kryoelektronmikroskop har fått stöd av Wallenbergstiftelsen och används i dag så flitigt att ett tredje är på väg Stockholm.
Ser proteiner i atomupplösning
Forskargruppens arbete kan beskrivas som en process i flera steg. Först renas molekylerna i mitoribosomerna fram för att fixeras i vatten som frusits så snabbt att det mer liknar glas, så kallat vitrifierat vatten. Därefter bombarderas provet med elektroner i ett mikroskop som fångar upp de oerhört svaga reflektionerna från varje molekyl.
Resultatet är tusentals bilder som genom en krävande bildbehandling kan kombineras samman till en tredimensionell karta som visar byggnadsblocken av varje molekyl.
Vid den punkt då provet fryses ned är molekyler fullt upptagna i sitt arbete, som att addera en aminosyra till ett protein, släppa en färdig proteinkedja fri, eller att bygga själva mitoribosomen. Alla dessa arbetsuppgifter går att urskilja och kombineras till en animerad sekvens av bilder, likt en film.
– När vi ser filmen kan vi börja fundera över hur de olika utvecklingsstadierna passar ihop och hur de länkas samman.
Stora mängder data
Mikroskopet genererar enorma mängder data, fyra terabyte per dag, som sparas ned på hårddiskar och bärs tre våningar upp för analys.
– De enorma mängderna data som produceras gör tillgången till beräkningskraft allt viktigare, säger Alexey Amunts.
Även om datorernas smarta algoritmer står för arbetet att kombinera bilderna rätt, så är det upp till forskarna att använda informationen för att bygga modeller av molekylerna på atomnivå. Och att tolka den för att öka förståelsen av hur mitoribosomernas uppbyggnad gör det möjligt för cellerna att bibehålla en energibalans.
Rasmus Kock Flygaard är en postdoktorand i gruppen och sitter djupt koncentrerad vid skärmen.
– Eftersom vi bygger något som aldrig skapats tidigare börjar jag med något som liknar en skiss. Därefter ser jag till att gå tillbaka gång på gång för att addera rätt delar till den slutgiltiga formen, säger Rasmus Kock Flygaard.
Alexey Amunts står ett steg bakom honom och pekar ivrigt på skärmen.
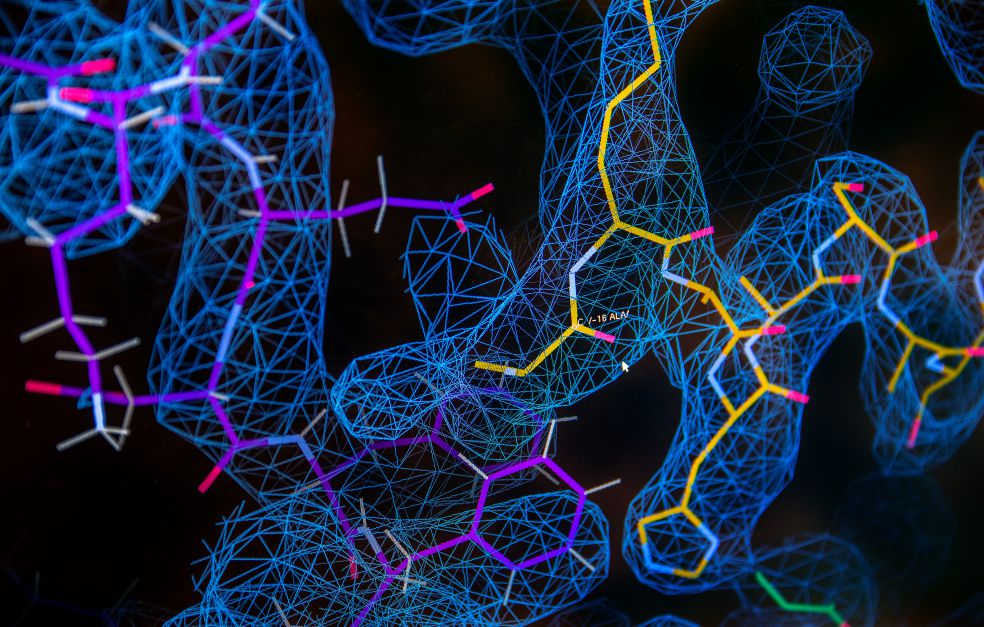
– Här ser du ett mellansteg i hur en ny mitoribosomstruktur växer fram. Detta är fortfarande opublicerade data och de delar av molekylen du ser här har ingen sett tidigare. Detta är ett exempel på de fundamentala upptäckter vi gör dagligen i labbet, säger Alexey Amunts och fortsätter:
– Det finns ingen mer belönande känsla för en strukturbiolog än att se hur de molekyler vi studerar är skulpterade enligt biokemins fundamentala lagar.
Bland de resultat som redan kommit ur projektet finns insikten om hur snabbt mitoribosomerna faktiskt kan syntetisera proteiner. Men utan projektanslaget från Knut och Alice Wallenbergs Stiftelse hade detta ambitiösa projekt inte varit möjligt, menar Alexey Amunts.
– Den femåriga projekttiden ger unika förutsättningar till en gemensam ansats för att undersöka nya, stora frågor som inte kan besvaras på en kortare tid.
Tillgången till forskningsanslaget var också en av anledningarna till att han valde Stockholms universitet framför det erkända labbet i Cambridge.
– Det långsiktiga stödet gör det möjligt att locka mycket begåvade människor och att skapa en miljö där de kan fokusera utan att behöva ta hänsyn till tid eller resurser. Upptäckterna vi gör har sin grund i den kultur och forskningsfrihet som anslaget kan bidrar till att skapa.
Text Magnus Trogen Pahlén
Bild Magnus Bergström