Projektanslag 2017
The Achilles’ heel of breast cancer
Huvudsökande:
Dr Anita Göndör
Medsökande:
Jonas Bergh
Lars Holmgren
Rolf Olsson
Jesper Tegner
Lärosäte:
Karolinska Institutet
Beviljat anslag:
36,8 miljoner kronor under fem år
Tumörceller kan invadera omgivande normal vävnad, överleva i blodcirkulationen och bilda metastaser i andra organ i kroppen. De är helt enkelt extremt bra på att anpassa sig till olika miljöer. På något sätt kan cancercellerna förändra sig i högre grad än normala celler, vilket gör det möjligt för dem att överleva och utvecklas i förändrade förhållanden.
Denna anpassningsförmåga bidrar till att göra cancerceller farliga. Men eftersom anpassningsförmågan är en egenskap som skiljer cancerceller från normala celler, skulle den också kunna användas som ett vapen mot dem. Den strategin undersöks i ett projekt vid Karolinska Institutet, KI, med anslag från Knut och Alice Wallenbergs Stiftelse.
– Eftersom dagens cancerbehandlingar inte slår mot tumörens mest karaktäristiska drag –dess förmåga till anpassning – kan tumörer tyvärr utveckla resistens mot de flesta behandlingar. Vi vill klarlägga mekanismen som driver anpassningsförmågan för att kunna utveckla nya sätt att behandla cancer, säger Anita Göndör.
Förklaringen tror de ligger i förändringar i hur arvsmassan är organiserad i cellens kärna.
Väcker tystade gener
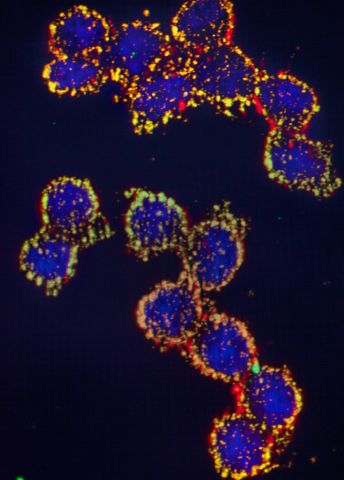
I cellkärnan är arvsmassan veckad i en struktur som kallas kromatin. Kromatin som innehåller aktiva gener tenderar att finnas i kärnans mitt. Genregioner som ska vara avstängda tenderar däremot att vara i utkanten av kärnan, i en miljö som motverkar genaktivering.
Denna separering är viktig för att behålla de egenskaper cellen får under normal utveckling. Men i cancerceller är systemet rubbat. Kontakten mellan inaktiva och aktiva regioner ökar och cellens mekanismer för att bevara cellernas egenskaper, dess epigenetiska tillstånd, blir instabila.
– Cellen hamnar i ett tillstånd av minnesförlust. Vår hypotes är att det möjliggör uppkomsten av cancerceller med olika egenskaper, vilket sedan driver tumörutvecklingen.
Nyligen har det visats att aktivering av gener som normalt bara är påslagna i tidiga embryonala cellstadier, är kopplad till bildandet av omogna, stamcells-liknande cancerceller som kan driva på tumörutvecklingen.
KI-forskarna vill undersöka om detta kan förklaras av att kromatinet i utkanten av cellkärnan förstörs, vilket de tror kan ske på grund av förändringar i cellmiljön, som exempelvis inflammation och åldrande.
Bättre behandling av bröstcancer
I projektet ska forskarna karaktärisera vad det är i arvsmassans tredimensionella organisation som driver det föränderliga beteendet hos tumörvävnaden. Förhoppningen är att hitta markörer för cancercellernas förändringsförmåga som kan användas för att mer precist klassificera tumörers beteende och sjukdomens prognos.
– Vi hoppas kunna förutsäga hur tumören kommer att bete sig i patienten bättre, att kunna förutsäga aggressivitet och risk för behandlingsresistens. Det vore intressant inte minst för en tidig form av bröstcancer, där vi vet att vissa av patienterna kommer att utveckla en mer avancerad sjukdom. I dag saknar vi metoder för att identifiera vilka det är.
Forskarna vill också undersöka hur cellernas anpassningsförmåga bidrar till att de kan undkomma kemoterapi. Tumörceller har egenheten att kunna gå in i en vilande fas, där de kan befinna sig i flera år utan att dela sig. Eftersom kemoterapi är inriktad på delande celler kan de därigenom undkomma behandlingen, för att en lång tid senare återaktiveras och orsaka metastaser.
I dag är endast lite känt om detta vilande tillstånd och hur cellerna kan gå ut och in ur det. Det vill KI-forskarna ändra på.
– Vår hypotes är att även om cellerna är vilande genomgår de någon sorts evolution och blir mer och mer plastiska. Vi ska karaktärisera arvsmassans tredimensionella organisering i det vilande tillståndet, för att förstå hur den bidrar till cellernas förändring och om vi på något sätt kan förhindra det.
Kräver bred kompetens
Anita Göndör försjunker en stund i en bild på mikroskopets skärm. Bilden visar proteinkomplex som reglerar hur en del av arvsmassan interagerar med en annan, avlägset belägen, region i cellkärnans yttre.
Metoder för att kunna kartlägga arvsmassans tredimensionella struktur på olika sätt är avgörande för projektet. Gruppens forskare har utvecklat tekniker som kan göra det i små cellpopulationer och enstaka celler, vilket krävs för analys av tumörmaterial.
I projektet vill forskarna ha en helhetssyn på cellen och undersöka hur dess reglerande lager kommunicerar med varandra. I gruppen ingår därför forskare med kompetens inom olika aspekter av cancerutveckling. Här finns klinisk kunskap, såväl som expertis inom exempelvis kromatin, biomekanisk signalering, cellmetabolism och inte minst avancerad beräkningsbiologi för att analysera all data som genereras.
Anita Göndör berättar om arbetet med entusiasm. Hon konstaterar att ingen tidigare har kartlagt de förändringar som sker i den tredimensionella organiseringen avarvsmassan i stamcells-liknande cancerceller. Anslaget är långsiktigt nog för att de ska våga försöka.
– Med det här stödet kan vi tänka bredare - ställa forskningsfrågor med hög risk och hög möjlig vinst. Svaren kan leda till något väldigt nytt.
Text Sara Nilsson
Bild Magnus Bergström